Рак молочной железы: причины онкологии, симптомы по стадиям, выживаемость и лечение

Фото: 5-tv.ru
Рак груди — одно из самых распространенных онкологических заболеваний.
Рак молочной железы (РМЖ) остается одной из самых актуальных проблем современной онкологии. По данным ВОЗ, это наиболее распространенный вид рака среди женщин во всем мире: ежегодно диагностируется более двух миллионов новых случаев.
Несмотря на прогресс в диагностике и лечении, заболевание продолжает занимать лидирующие позиции в структуре онкологической смертности.
Вместе с тем ранняя диагностика и персонализированный подход к терапии позволяют добиться высоких показателей выживаемости: на I–II стадиях пятилетняя выживаемость достигает 90%.
Понимание механизмов развития болезни, знание факторов риска и симптомов, а также грамотное планирование реабилитации после лечения — ключевые элементы успешной борьбы с раком груди.
Как возникает рак молочной железы
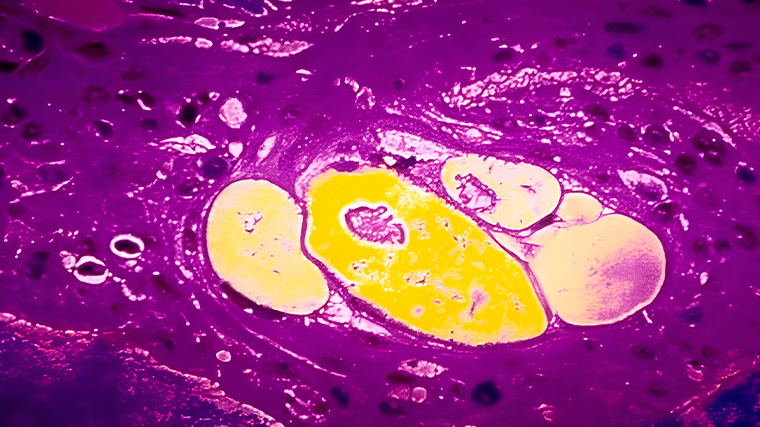
Рак груди развивается так же, как и любая другая злокачественная опухоль. В основе развития рака лежит повреждение ДНК — молекулы, которая содержит «инструкции» по строению и работе клеток.
Когда в ДНК накапливается достаточно изменений, клетка становится злокачественной: перестраивает метаболизм, начинает быстро делиться и расти, захватывая все больше тканей.
Сбои в ДНК могут возникать по разным причинам: из-за генетической предрасположенности, воздействия радиации, вредных химических веществ, инфекций или гормональных нарушений. Со временем из таких дефектных клеток формируется опухоль.
Часто рак молочной железы относится к категории аденокарцином — опухолей из железистого эпителия. Они развиваются внутри протоков молочных желез, постепенно разрастаясь и захватывая все большее количество тканей.
Без лечения опухоль может прорастать в окружающие ткани, а злокачественные клетки — отсоединяться от нее и распространяться по организму через лимфатическую и кровеносную систему.
Они поражают сначала ближайшие лимфатические узлы (подмышечные, подключичные, надключичные), а затем могут метастазировать в легкие, печень, головной мозг, кости и другие органы. Именно метастазы часто становятся причиной гибели пациентов, поскольку нарушают работу жизненно важных систем.
Типы рака молочной железы
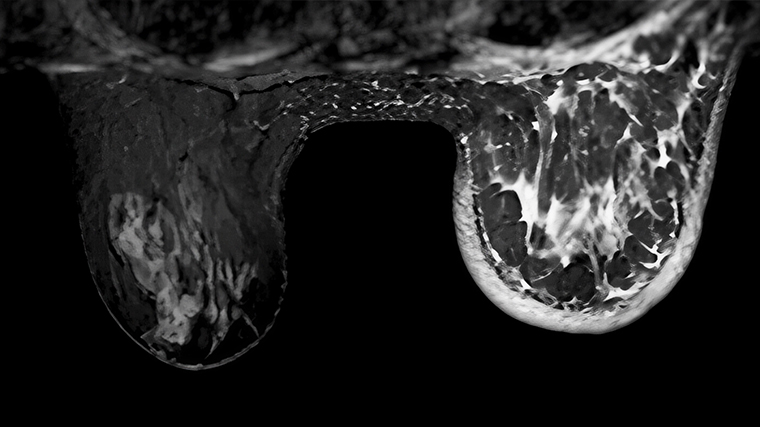
Рак молочной железы — не единое заболевание, а целая группа опухолей с разным поведением, прогнозом и реакцией на лечение. Опухоль обязательно проверяют на рецепторы к эстрогену и прогестерону, а также на белок HER2 (рецептор эпидермального фактора роста второго типа). От этого зависит стратегия лечения.
Анатомическая классификация рака молочной железы:
- Инвазивная протоковая карцинома (70–80% случаев). Опухоль зарождается в молочных протоках и прорастает в окружающие ткани. Прогноз зависит от стадии обнаружения и молекулярных особенностей опухоли.
- Инвазивная дольковая карцинома. Начинается в дольках, вырабатывающих молоко. Часто растет «рассеянно», без четкого узла — из‑за этого ее сложнее выявить на ранней стадии даже при маммографии. Для диагностики может потребоваться МРТ.
- Неинвазивный рак (DCIS, протоковая карцинома in situ). Злокачественные клетки есть, но они не вышли за пределы протока — это нулевая стадия. При своевременном лечении прогноз очень хороший: болезнь обнаруживают фактически «в зародыше».
- Воспалительный рак груди. Редкая, но крайне агрессивная форма. Симптомы: покраснение, отек, уплотнение кожи (она становится похожа на апельсиновую корку). Его часто путают с маститом или аллергией, из‑за чего теряется драгоценное время. Требуется быстрая диагностика и немедленное комбинированное лечение.
Молекулярные подтипы рака молочной железы:
- Гормонопозитивный (люминальный) рак (примерно 70% случаев):
- Люминальный A. Наиболее благоприятный вариант: высокая чувствительность к гормонам (ER+, PR+), низкий уровень Ki-67 (медленное деление клеток), HER2-отрицательный. Обычно достаточно гормональной терапии, химиотерапия нужна редко. Имеет лучший прогноз, чем B.
- Люминальный B. Более агрессивный: ER+, но PR может быть снижен, высокий Ki-67, может быть HER2-позитивным. Требует комбинированного лечения: гормонотерапии + химиотерапии, иногда — таргетных препаратов.
- HER2-положительный рак. Раньше считался одним из самых агрессивных, но с появлением таргетных препаратов (трастузумаб и др.) прогноз значительно улучшился. Опухоль имеет гиперэкспрессию HER2-рецептора, что позволяет прицельно воздействовать на нее специальными лекарствами.
- Трижды негативный рак (15–17% случаев). Самый сложный для лечения вариант:
- нет рецепторов к эстрогенам и прогестерону;
- нет HER2-рецепторов;
- не реагирует на гормонотерапию и таргетные препараты против HER2;
- часто встречается у носительниц мутаций BRCA1;
- требует интенсивной химиотерапии, в новых протоколах используют иммунотерапию.
Причины рака молочной железы

В основе развития рака лежит повреждение ДНК — молекулы, которая содержит «инструкции» по строению и работе клеток. Когда в ДНК накапливается достаточно изменений, клетка становится злокачественной: перестраивает метаболизм, начинает быстро делиться и расти, захватывая все больше тканей.
Сбои в ДНК могут возникать по разным причинам:
- Генетические мутации. Около пяти-десяти процентов случаев РМЖ связаны с наследственными мутациями в генах BRCA1 и BRCA2. Эти гены отвечают за репарацию (восстановление) поврежденной ДНК. При их мутации клетки накапливают еще больше мутаций, что может привести к раку.
- Гормональные нарушения. Длительное воздействие эстрогенов и прогестерона повышает риск. Это связано с ранним началом менструаций (до 12 лет), поздней менопаузой (после 55 лет), поздними первыми родами (после 30 лет) или их отсутствием.
- Воздействие радиации. Лучевая терапия в области грудной клетки, особенно в возрасте до 30 лет (например, при лечении лимфомы Ходжкина), увеличивает риск развития РМЖ в будущем.
- Химические вещества и токсины. Некоторые химические вещества, которые могут содержаться в окружающей среде или на производстве, потенциально провоцируют развитие опухолей.
Факторы риска делят на немодифицируемые (на которые нельзя повлиять) и модифицируемые (их влияние можно уменьшить изменением образа жизни).
Немодифицируемые факторы:
- Возраст. Риск значительно возрастает после 40–50 лет. С возрастом в клетках накапливаются генетические изменения, а эффективность работы иммунной системы снижается.
- Генетическая предрасположенность. Наличие мутаций в генах BRCA1, BRCA2, CHEK и других повышает риск. Если в семье были случаи рака груди или яичников, стоит сдать генетический тест.
- Личный анамнез. Если у женщины уже был диагностирован РМЖ в возрасте до 40 лет, вероятность рецидива или развития новой опухоли значительно увеличивается.
- Высокая плотность молочной железы. Этот показатель определяется при маммографии. Чем больше в ткани молочной железы железистой и фиброзной ткани, тем выше плотность и риск развития рака.
- Раса и этническое происхождение. У женщин европеоидной расы РМЖ встречается чаще, чем у чернокожих. При этом у последних такие опухоли чаще диагностируются до 45 лет и характеризуются более высокой смертностью. Среди азиатских женщин и распространенность, и смертность от РМЖ ниже.
- Рост. По неизвестным причинам рак груди несколько чаще встречается у высоких женщин.
Модифицируемые факторы:
- Избыточный вес и ожирение. Особенно опасно ожирение в постменопаузе: жировая ткань начинает активно вырабатывать эстрогены, что повышает риск.
- Низкая физическая активность. Сидячая работа и малоподвижный образ жизни удваивают риск по сравнению с активными женщинами.
- Курение и алкоголь. Курение повышает риск на 20%, а даже один бокал вина в день — на 7–10%. Алкоголь может повреждать клеточную ДНК и увеличивать уровень эстрогена.
- Неправильное питание. Диета с избытком животных жиров и недостатком фруктов, овощей и зелени повышает риск.
- Заместительная гормональная терапия (ЗГТ) в менопаузе. Длительное применение гормонов (особенно комбинации эстрогена и прогестерона) увеличивает риск.
- Длительный прием комбинированных оральных контрацептивов (КОК). Риск немного повышается при приеме более 10 лет, но через 10 лет после прекращения приема он возвращается к обычному уровню.
- Отсутствие родов или поздние первые роды. У нерожавших женщин или при поздних первых родах (старше 30 лет) риск в 2–3 раза выше, чем у рожавших до 20 лет.
- Отсутствие грудного вскармливания. Кормление грудью снижает риск: за каждые 12 месяцев лактации риск уменьшается на 4–5%.
- Травмы молочных желез, мастит. Могут провоцировать воспалительные процессы, которые потенциально повышают риск.
Профилактика рака молочной железы
Профилактика включает три уровня: первичную, вторичную и третичную.
Первичная профилактика направлена на снижение риска через изменение образа жизни:
- Контроль веса. Поддерживать индекс массы тела (ИМТ) в пределах 18,5–24,9.
- Физическая активность. Рекомендуется не менее 150 минут умеренных нагрузок в неделю (ходьба, йога, плавание).
- Здоровое питание. Увеличить потребление фруктов, овощей, цельнозерновых продуктов, снизить потребление животных жиров.
- Отказ от вредных привычек. Бросить курить и ограничить употребление алкоголя.
- Грудное вскармливание. Кормить ребенка грудью минимум 6 месяцев при отсутствии противопоказаний.
- Избегание избыточной инсоляции. Загорать на солнце или в солярии только с закрытой грудью.
Вторичная профилактика — это ранняя диагностика:
- Самообследование. Проводить ежемесячно, начиная с 18–20 лет, в первые несколько дней после окончания менструации.
- Маммография. С 40 лет — каждые 2 года, после 50 лет — ежегодно. При наличии факторов риска (наследственность, атипичные изменения) — ежегодно с 35 лет.
- УЗИ молочных желез. По показаниям для женщин до 40 лет, во время беременности и лактации.
- Регулярные осмотры у маммолога и гинеколога. После 35–40 лет — ежегодно.
Третичная профилактика направлена на предотвращение рецидивов после лечения:
- Регулярное наблюдение у онколога или маммолога.
- Маммография и УЗИ по назначению врача.
- Анализ крови на онкомаркеры.
- Диагностическая пункция тканей груди — по показаниям.
Важно помнить, что даже при наличии нескольких факторов риска развитие рака не гарантировано, но их контроль значительно снижает вероятность заболевания.
Симптомы рака молочной железы

Рак молочной железы часто развивается бессимптомно на ранних стадиях, что затрудняет его своевременное обнаружение. Однако при появлении определенных признаков необходимо обратиться к маммологу для обследования.
Основные симптомы:
1. Уплотнение в груди. Это наиболее распространенный симптом. Уплотнение может быть безболезненным или вызывать дискомфорт, часто прощупывается под кожей, но не всегда заметно внешне.
2. Изменение формы или размера груди. Одна грудь может увеличиться, изменить свою форму по сравнению с другой, иногда это сопровождается тяжестью или отеком.
3. Выделения из соска. Могут быть кровянистыми или прозрачными.
4. Изменения кожи груди:
- появление «апельсиновой корки» (плотной и неровной кожи из-за нарушения лимфооттока);
- покраснение, шелушение или воспаление;
- втяжение кожи над очагом поражения.
5. Изменение формы соска. Он может втянуться внутрь, а кожа вокруг него начать шелушиться. При раке Педжета сосок может стать выпуклым и утолщенным.
6. Боль и дискомфорт в груди. На ранних этапах опухоль часто не проявляет себя болями, но по мере прогрессирования заболевания могут появиться болезненные ощущения.
7. Увеличенные и болезненные лимфоузлы в подмышечной области. При развитии заболевания могут прощупываться уплотненные лимфоузлы.
Общие симптомы онкологических заболеваний:
- беспричинная потеря веса;
- повышенная утомляемость;
- отеки, особенно ног;
- ломота в костях.
Симптомы при метастазах:
Если рак метастазирует в другие органы, симптомы могут быть разными:
- при метастазах в кости — боли в спине, ногах;
- при поражении печени — боль в правом подреберье, желтуха (пожелтение кожи и белков глаз);
- при поражении легких — одышка и кашель.
Важно помнить, что не каждая опухоль в молочной железе злокачественная. В большинстве случаев они доброкачественные и не опасны для жизни. Только врач может оценить значимость симптомов.
Многие из перечисленных признаков могут быть проявлениями других заболеваний. Регулярное самообследование и профилактические осмотры (маммография после 40 лет — не реже раза в год) помогают выявить проблему на ранней стадии.
Особенности некоторых форм рака груди
Диффузные формы (отечно-инфильтративные):
- грудь увеличена в размерах, уплотнена;
- кожа покрасневшая, горячая на ощупь;
- боль распространяется на всю железу;
- эффект «лимонной корки» наблюдается по всей поверхности органа;
- сосок и ареола утолщены, иногда наблюдается его втяжение и фиксация в таком положении;
- иногда повышается температура тела, присоединяется слабость, вялость.
Рак Педжета:
- на поверхности кожи соска или ареолы появляется покраснение, образуются корки (сухие или мокнущие), иногда возникает шелушение;
- женщина может ощущать зуд, пощипывание, повышенную чувствительность соска;
- позже меняется конфигурация соска: он втягивается или становится выпуклым и утолщенным;
- в некоторых случаях появляется серозное отделяемое из протоков;
- при развитии патологического процесса могут возникать изъязвления, мокнущие эрозии, боль и жжение в области соска;
- увеличиваются и уплотняются подмышечные лимфоузлы.
Как проводить самообследование рака молочной железы
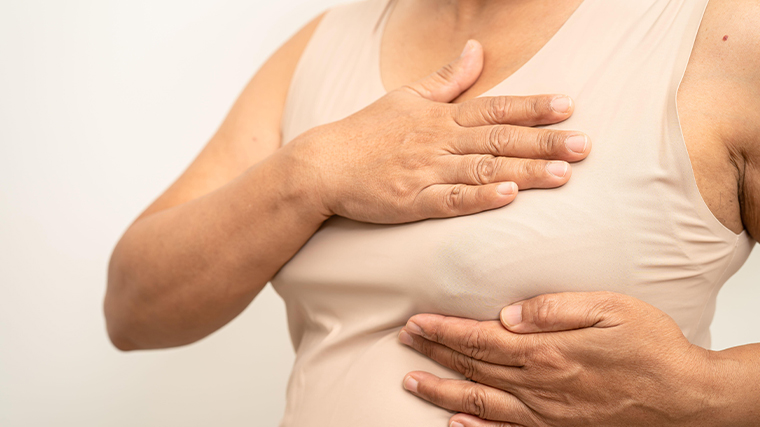
Самообследование молочных желез — это регулярный осмотр и пальпация груди, которые помогают вовремя заметить изменения и при необходимости обратиться к врачу. Однако важно понимать, что самообследование не заменяет профессиональную диагностику у маммолога, УЗИ, маммографии или других инструментальных методов.
Рекомендуется выполнять процедуру ежемесячно. Женщинам с регулярным менструальным циклом оптимальное время — через пять–семь дней после начала месячных, когда грудь наименее чувствительна и отечна. В период менопаузы или при нерегулярном цикле следует выбрать фиксированный день месяца. Регулярное самообследование особенно важно для женщин из групп риска: с наследственной предрасположенностью (мутации BRCA½), возрастом старше 40 лет, с гормональными нарушениями, отсутствием беременностей, абортами, отказом от грудного вскармливания.
Самообследование помогает заметить изменения, но не заменяет профессиональную диагностику. Только врач может определить, являются ли обнаруженные изменения доброкачественными или злокачественными. Также важно понимать, что некоторые опухоли могут быть совсем маленькими и не прощупываться.
Как проводить самообследование:
1. Осмотр белья. Проверьте нижнее белье на наличие выделений из сосков — даже небольшие выделения могут оставлять следы.
2. Визуальный осмотр перед зеркалом. Встаньте прямо, опустите руки вдоль тела. Осмотрите каждую молочную железу, обращая внимание на симметричность груди (они должны располагаться на одном уровне, соски и нижние границы — на одном уровне), изменения размера, формы, контуров, состояние кожи (покраснения, шелушение, сыпь, участки уплотнения, «лимонной корки» — утолщения кожи с ямочками) и форму и состояние сосков (втяжение, деформация, изъязвление, шелушение). Потом поднимите руки над головой и повторите осмотр.
3. Пальпация стоя. Лучше проводить во время душа — намыленные руки облегчают скольжение. Левой рукой ощупывайте правую грудь, правой — левую. Используйте подушечки трех сомкнутых пальцев (указательного, среднего, безымянного), а не кончики. Движения должны быть круговыми, пружинящими, проникающими вглубь тканей. Обследуйте всю грудь, двигаясь от ключицы к ребрам и от середины грудной клетки к подмышечной впадине.
4. Пальпация лежа. Лягте на спину, под исследуемую грудь можно подложить валик или свернутое полотенце. Есть два метода:
- Квадратный. Мысленно разделите переднюю часть грудины (от ключицы до нижнего края ребер) на квадраты. Прощупывайте каждый квадрат последовательно, сверху вниз.
- Спиральный. Двигайтесь по спирали — от подмышечной впадины к соску.
5. Обследование сосков. Слегка сожмите сосок у основания большим и указательным пальцами. Проверьте, есть ли выделения, и отметьте их характер (цвет, консистенция).
6. Осмотр подмышечных впадин. Прощупайте лимфоузлы круговыми движениями. В норме они не должны быть увеличены или болезненны.
Немедленно обратитесь к маммологу, если обнаружили новое уплотнение или шишку, которая не исчезает; , асимметрию груди или внезапное изменение ее формы, втяжение кожи или соска, необычные выделения из соска, особенно кровянистые, покраснение, уплотнение или шелушение кожи груди, болезненность, которая сохраняется и усиливается без связи с менструальным циклом, а также увеличение лимфоузлов в подмышечной области.
Небольшие изменения, которые появляются периодически, могут быть связаны с гормональными колебаниями. Но любые новые признаки требуют консультации врача.
Диагностика рака молочной железы у врача

Диагностика рака молочной железы у врача включает несколько этапов: сбор анамнеза, осмотр, инструментальные и лабораторные исследования, а также биопсию для окончательного подтверждения диагноза.
Диагностика начинается с беседы с врачом. Специалист выясняет жалобы пациентки, наличие факторов риска (например, гормональные нарушения, возраст, ожирение) и семейную предрасположенность к раку молочной железы. Важно уточнить, были ли случаи заболевания в семье, так как это может указывать на наследственную форму, связанную с мутациями в генах BRCA1, BRCA2, NBS1, CHECK, TP53.
Дальше врач осматривает молочные железы в положении стоя и лежа, оценивает их симметричность, состояние кожи и сосков. При пальпации специалист прощупывает грудь по часовой стрелке, проверяя наличие уплотнений, узлов или болезненных участков. Также врач пальпирует подмышечные, надключичные и подключичные лимфатические узлы, чтобы определить, увеличены ли они.
После может последовать маммография или другой вид инструментальной диагностики:
- Маммография — рентгенологическое исследование молочных желез в двух проекциях. Метод позволяет обнаружить опухоли диаметром от 0,5 сантиметра, определить их локализацию, размер и форму. Признаки злокачественности: нечеткие границы, неправильная форма, наличие кальцинатов внутри новообразования. Маммография чаще применяется у женщин после 35–40 лет.
- Ультразвуковое исследование (УЗИ) используется, особенно у женщин до 35 лет. Метод помогает отличить кисты (полости с жидкостью) от плотных опухолей, оценить состояние лимфатических узлов и контролировать положение иглы во время биопсии.
- Магнитно-резонансная томография (МРТ) применяется в сложных случаях: при лобулярном раке, когда маммография и УЗИ неинформативны, при мутациях генов BRCA, высокой плотности ткани молочной железы, наличии имплантов. МРТ дает детальное изображение мягких тканей, помогает оценить размеры и расположение опухоли, что важно для планирования хирургического лечения.
- Дуктография (галактография) — рентгенография с контрастированием молочных протоков. Метод используется при кровянистых выделениях из соска для выявления патологий в протоках.
- ПЭТ-КТ (позитронно-эмиссионная компьютерная томография) применяется для выявления метастазов. Это исследование с контрастированием позволяет обнаружить участки с наиболее активным клеточным делением.
- СВЧ-радиотермосканирование позволяет оценить колебания температуры тканей молочных желез на глубине до 14 сантиметров. Раковые очаги обладают более высокой температурной активностью из-за быстрого деления клеток.
В лабораторную диагностику входят общий и биохимический анализы крови, коагулограмма, общий анализ мочи (помогают оценить общее состояние здоровья и выявить неспецифические изменения (повышение СОЭ и уровня лейкоцитов, снижение гемоглобина и эритроцитов, рост С-реактивного белка)), анализ на онкомаркер СА 15-3 (используется для мониторинга течения заболевания и оценки эффективности лечения.
У этого маркера низкая специфичность, поэтому положительный результат не всегда указывает на рак), а также генетические тесты — определение мутаций в генах BRCA1, BRCA2 методом ПЦР или NGS для выявления наследственной предрасположенности.
Ключевым методом окончательного подтверждения диагноза является биопсия. Она позволяет определить тип опухоли, ее биологические характеристики (например, наличие рецепторов к эстрогену и прогестерону, HER-2-статус, индекс пролиферативной активности ki67) и подобрать тактику лечения.
Виды биопсии:
- Тонкоигольная биопсия — забор клеток с помощью иглы под контролем УЗИ или маммографии.
- Трепанобиопсия (CORE-биопсия) — использование специального инструмента, напоминающего толстую полую иглу, для получения большего количества ткани.
- Биопсия «пистолет-игла» — точное введение иглы с помощью специального пистолета.
- Стереотаксическая вакуум-биопсия — высокоточный метод, выполняемый под местной анестезией с помощью пистолета Bard Magnum и вакуум-аппарата.
- Эксцизионная биопсия — удаление всей опухоли вместе с тканями молочной железы во время хирургического вмешательства.
- Сентинель-биопсия — исследование сторожевого лимфатического узла во время операции для определения распространения опухоли на лимфоузлы.
После подтверждения диагноза важно определить стадию заболевания. Для этого используют УЗИ и биопсию лимфатических узлов, КТ и МРТ для оценки размеров и расположения опухоли, поиска очагов в других органах, рентгенографию для выявления метастазов в легких и костях и сцинтиграфию при подозрении на распространение злокачественных клеток в костную ткань.
Стадирование проводится по системе TNM, где T обозначает размер первичной опухоли, N — вовлечение лимфатических узлов, M — наличие отдаленных метастазов. Важно помнить, что только врач может интерпретировать результаты исследований и поставить точный диагноз.
Стадии рака молочной железы

Стадирование рака молочной железы — это способ оценить, насколько распространилась опухоль в организме. На его основе врачи выбирают тактику лечения и прогнозируют исход болезни. Для этого используют международную систему TNM, где:
- T (tumor) отражает размер и распространение первичной опухоли;
- N (nodules) показывает, поражены ли лимфатические узлы;
- M (metastasis) фиксирует наличие отдаленных метастазов.
0 стадия (карцинома in situ) — это «рак на месте»: злокачественные клетки присутствуют, но не выходят за пределы протока или дольки молочной железы (DCIS или LCIS). Опухоль микроскопическая, не прорастает в окружающие ткани, лимфоузлы не затронуты, метастазов нет. Часто ее обнаруживают случайно во время профилактического обследования. Прогноз очень благоприятный: при своевременном лечении выздоровление наступает почти в 100% случаев.
I стадия означает, что опухоль уже прорастает в соседние ткани, но остается небольшой: ее размер не превышает 2 см (T1). Лимфоузлы либо не затронуты (N0), либо поражены микроскопически (N1mi), а метастазов по‑прежнему нет (M0). На этом этапе уплотнение может прощупываться, но зачастую жалоб у женщины нет. Шансы на полное излечение высоки: 5‑летняя выживаемость составляет около 98–100%.
II стадия делится на две подстадии — IIA и IIB — и характеризуется ростом опухоли и возможным вовлечением ближайших лимфоузлов. При IIA опухоль либо не превышает двух сантиметров, но затрагивает от одного до трех подмышечных лимфоузлов, либо имеет размер в два-пять сантиметров при чистых лимфоузлах. На стадии IIB опухоль также составляет два-пять сантиметров, но уже поражает один-три лимфоузла, либо превышает пять см, оставаясь без поражения лимфоузлов. В этот период могут появиться асимметрия груди, изменения кожи или увеличение лимфоузлов. При комплексном лечении пятилетняя выживаемость достигает 80–90%.
III стадия свидетельствует о серьезном распространении процесса и подразделяется на IIIA, IIIB и IIIC. На IIIA опухоль может быть любого размера, но поражает четыре-девять лимфоузлов (в подмышке или около грудины), возможен отек молочной железы. IIIB характеризуется прорастанием опухоли в кожу или грудную стенку, что проявляется симптомом «лимонной корки», иногда возникают изъязвления кожи; лимфоузлы поражены, но отдаленных метастазов еще нет. IIIC отличается поражением десяти и более лимфоузлов, включая надключичные, при любом размере опухоли. Симптомы становятся заметными: грудь деформируется, появляется отек, покраснение, выделения из соска, увеличиваются лимфоузлы. Прогноз сложнее, чем на ранних стадиях, но лечение возможно: пятилетняя выживаемость варьируется от 50 до 70% в зависимости от подстадии.
IV стадия (метастатический рак) — самая тяжелая форма заболевания, при которой опухоль распространяется на другие органы. Здесь уже фиксируются отдаленные метастазы (M1), чаще всего поражающие кости, легкие, печень или головной мозг. Размер первичной опухоли и степень поражения лимфоузлов могут быть любыми. Болезнь переходит в хроническую форму: полное излечение маловероятно, но грамотное лечение позволяет контролировать состояние и продлевать жизнь. Симптомы зависят от пораженных органов: боли и переломы при метастазах в кости, одышка и кашель — в легких, желтуха и тяжесть в правом боку — в печени, головные боли и нарушения координации — в головном мозге. Средняя пятилетняя выживаемость на этой стадии составляет около 25–30%, но многие пациенты живут годами при правильно подобранной терапии.
Прогноз при раке молочной железы
Прогноз при раке молочной железы (РМЖ) — это статистическая оценка вероятности выздоровления или длительной ремиссии. Он не предсказывает судьбу конкретного человека, но помогает врачам и пациентам понять перспективы лечения.
Стадия на момент диагностики — самый важный фактор.
- 0–I стадия: пятилетняя выживаемость около 98–100%;
- II стадия: около 80–90%;
- III стадия: около 50–70% (зависит от подстадии и молекулярного подтипа);
- IV стадия: около 25–30%.
Молекулярный подтип опухоли (определяется по рецепторам ER, PR, HER2 и индексу Ki‑67):
- Люминальный A (ER+/PR+, HER2–, низкий Ki‑67): наиболее благоприятный прогноз, хорошо отвечает на гормональную терапию.
- Люминальный B (ER+/PR±, HER2+, высокий Ki‑67): агрессивнее, требует комбинированного лечения (гормонотерапия + химио-/таргетная терапия).
- HER2‑положительный: раньше считался неблагоприятным, но с появлением таргетных препаратов (трастузумаб и др.) прогноз значительно улучшился.
- Трижды негативный (ER–, PR–, HER2–): самый агрессивный, склонен к рецидивам в первые 3–5 лет, но при отсутствии рецидива после этого срока прогноз улучшается.
Степень злокачественности (G):
- G1 (низкая): клетки похожи на нормальные, растут медленно;
- G2 (умеренная): промежуточный вариант;
- G3 (высокая): клетки сильно отличаются от нормальных, быстро делятся — прогноз хуже.
Возраст и общее состояние здоровья:
- молодые женщины (до 35 лет) чаще имеют агрессивные формы;
- сопутствующие заболевания (диабет, сердечно‑сосудистые патологии) могут ограничивать выбор терапии.
Генетические факторы:
- мутации BRCA½ ассоциированы с более высоким риском рецидива, но не всегда ухудшают прогноз при грамотном лечении;
- другие генетические маркеры (например, PIK3CA) помогают подобрать таргетную терапию.
Ответ на лечение:
- полный патоморфологический ответ (исчезновение опухоли после неоадъювантной терапии) улучшает прогноз;
- резистентность к терапии ухудшает его.
Локализация и количество метастазов (для IV стадии):
- единичные метастазы в кости — более благоприятный вариант;
- множественные поражения печени, легких или мозга — прогноз хуже.
Данные о реальных цифрах выживаемости основаны на популяционных исследованиях и регистрах (например, SEER в США, EUROCARE в Европе). Эти цифры усредненные. В последние годы они улучшаются благодаря новым методам лечения (иммунотерапия, таргетные препараты).
Пятилетняя относительная выживаемость (сравнивается с общей популяцией):
- локализованный рак (0–I стадия) — 99%;
- местнораспространенный (II–III стадия) — 86%;
- метастатический (IV стадия) — 30%.
Десятилетняя выживаемость:
- I стадия — 85–90%;
- II стадия — 65–80%;
- III стадия — 40–60%;
- IV стадия — около 10–15%.
За последние 20 лет прогноз улучшился благодаря ранней диагностике, персонализированной терапии, новым препаратам и комплексному подходу.
Лечение рака молочной железы
Лечение рака молочной железы подбирается индивидуально с учетом стадии заболевания, биологического подтипа опухоли, состояния здоровья пациентки и ее личных предпочтений.
Современная медицина использует комплекс методов, которые могут применяться как по отдельности, так и в сочетании для достижения наилучших результатов.
Хирургическое вмешательство — основной метод борьбы со злокачественными опухолями молочной железы, особенно на ранних стадиях.
Виды операций:
- Органосохраняющие операции (лампэктомия, секторальная резекция). Хирург удаляет только опухоль и небольшой участок здоровой ткани вокруг нее. Применяется на ранних стадиях, когда опухоль небольшая. После такой операции часто назначается лучевая терапия для уничтожения оставшихся раковых клеток.
- Мастэктомия. Удаляется вся пораженная молочная железа. Может быть полной (простая мастэктомия), радикальной (мастэктомия по Холстеду) или модифицированной (мастэктомия по Маддену). К мастэктомии обычно прибегают, если органосохраняющая операция не может быть выполнена, при подтвержденной наследственной предрасположенности или если пациент настаивает на полном удалении.
- Диссекция лимфоузлов. Процедура, при которой удаляют один, несколько или все лимфоузлы в подмышечной области. Обычно выполняется вместе с операцией на молочной железе и показана пациентам с раком молочной железы, при котором выявлены метастазы в лимфоузлах.
Иногда проводится профилактическая мастэктомия у женщин с высоким риском заболевания, чтобы снизить вероятность развития рака.
Чтобы разобраться, распространились ли раковые клетки в лимфатические узлы, и определиться с объемом хирургического вмешательства, может быть проведена сентинель-биопсия (биопсия сторожевого лимфоузла).
Во время операции в опухоль вводят радиофармпрепарат или флуоресцентный краситель — это помогает визуализировать лимфоузел, который первым принимает лимфу от ткани молочной железы. Его удаляют и проводят гистологическое исследование.
Если в сторожевом лимфоузле не обнаруживают опухолевых клеток, можно ограничиться удалением очага в молочной железе. В противном случае показано иссечение регионарных лимфоузлов
После хирургического удаления возможно восстановление формы молочной железы с помощью реконструктивной маммопластики. Для этого врач использует импланты или собственные ткани пациентки, например из области живота или спины.
Лучевая терапия основана на разрушении злокачественных клеток путем воздействия на них ионизирующего излучения. Обычно ее совмещают с хирургическими методиками, но в некоторых случаях применяют отдельно.
Виды лучевой терапии:
- Неоадъювантная. Проводится до операции. Уменьшает объем новообразования, уничтожает злокачественные клетки по периферии облучаемой области. Позволяет перевести неоперабельный рак в операбельный, уменьшить вероятность рецидива.
- Адъювантная. Назначается после операции. Приводит к гибели злокачественных клеток, которые могли быть не удалены при оперативном лечении.
- Интраоперационная. Заключается в воздействии облучения на открытую рану. Применяется для снижения рисков при органосохраняющем вмешательстве.
- Самостоятельная. Направлена на улучшение самочувствия пациента. Применяется при неоперабельном раке.
Лучевая терапия после операции часто назначается после частичного или полного удаления железы, чтобы предотвратить рецидив.
Химиотерапия — это лечение рака препаратами, обладающими противоопухолевой активностью. Подобные лекарства останавливают рост и провоцируют гибель активно делящихся клеток злокачественной опухоли.
Виды химиотерапии:
- Неоадъювантная. Помогает уменьшить размер опухоли перед вмешательством, повышает успех проведения операции, снижает вероятность рецидива после нее.
- Адъювантная. Проводится после операции, чтобы избавиться от оставшихся в организме раковых клеток и достичь полной ремиссии.
- Паллиативная. При отдаленных метастазах химиотерапия проводится как основной метод лечения. Она помогает замедлить прогрессирование, уменьшить симптомы, вызванные заболеванием, и продлить жизнь пациентки.
Химиотерапию проводят курсами. Количество курсов и схему лечения подбирает врач индивидуально.
Гормонотерапию назначают после подтверждения гормональной чувствительности опухоли. В заключении патоморфологического исследования должны быть указаны данные о рецепторах к эстрогену и/или прогестерону. Цель терапии — устранить гормональную стимуляцию и замедлить рост опухоли.
Основные подходы различаются по механизму действия. В одних схемах препарат блокирует гормональные рецепторы в раковых клетках: эстроген и прогестерон остаются в организме, но не могут активировать ростовые процессы. В других случаях снижают уровень эстрогена, чаще с помощью ингибиторов ароматазы. Этот подход особенно распространен у женщин после менопаузы.
Если функция яичников сохранена, их активность дополнительно подавляют медикаментозно, а при некоторых показаниях рассматривают хирургическое удаление яичников. Иногда методы комбинируют.
Таргетная, или прицельная, терапия — это современный метод лечения, который направлен на конкретные молекулы или механизмы в опухолевых клетках.
Показания к применению препаратов:
- выявление в новообразовании рецепторов HER2;
- распространенность очагов заболевания по организму;
- рецидив и диагностированные метастазы.
Примеры таргетных препаратов:
- Трастузумаб. Рекомбинантное моноклональное антитело, которое предотвращает развитие раковых клеток посредством связи с белком в клеточной мембране.
- Пертузумаб. Останавливает процесс соединения атипичных клеток друг с другом.
- Эверолимус. Замедляет активность белкового фермента mTOR, который отвечает за рост опухоли и сосудов в ней.
- Лапатиниб. Ингибирует сигнальные пути, отвечающие за рост и деление клетки.
Таргетные препараты применяются как часть комплексного лечения. С их помощью значительно улучшаются результаты хирургического, гормонального, а также химиотерапевтического этапов.
Иммунотерапия при раке молочной железы — это метод лечения, направленный на активацию иммунной системы для борьбы с опухолевыми клетками. Обычно иммунотерапию применяют для лечения трижды негативного рака, который не отвечает на гормональную и таргетную терапию.
Реабилитация после лечения рака молочной железы

Реабилитация после лечения рака молочной железы — это непрерывный процесс, который начинается сразу после операции или завершения основного курса терапии и может продолжаться месяцы или годы. Его цель — восстановить физическое и психоэмоциональное здоровье, минимизировать последствия лечения и вернуть женщину к полноценной жизни.
Сразу после операции внимание уделяется профилактике застойных явлений в легких через дыхательную гимнастику, а также легким движениям кистью и предплечьем, осторожным сгибаниям и разгибаниям руки в локте и самомассажу пальцев для стимуляции кровообращения (первые две-четыре недели). По мере заживления рубцов и стабилизации состояния программа расширяется: с первого по третий месяц постепенно увеличивают амплитуду движений в плечевом суставе, добавляют упражнения с резиновыми лентами сопротивления и легкую растяжку, включают ходьбу в комфортном темпе.
На этапе трех-шести месяцев вводят силовые упражнения с малыми весами, плавание (после заживления рубцов), занятия на тренажерах под контролем инструктора, йогу или пилатес для улучшения координации и баланса. После шести месяцев происходит возвращение к привычным физическим нагрузкам, но с обязательным контролем состояния конечности при интенсивных тренировках и регулярной самодиагностикой отека и болей.
Одна из частых проблем — лимфостаз (отек руки), возникающий из‑за нарушения оттока лимфы после удаления лимфоузлов. Для его коррекции носят компрессионный трикотаж с подобранным классом компрессии, выполняют ручной лимфодренажный массаж (под руководством специалиста), проходят курсы аппаратной пневмокомпрессии и лечебной физкультуры для стимуляции лимфотока. В тяжелых случаях прибегают к хирургическим методам — лимфовенозным анастомозам или пересадке лимфоузлов.
Параллельно решают проблему ограничения подвижности плечевого сустава через ежедневную гимнастику (круговые движения, подъемы рук, отведения), физиотерапевтические процедуры (магнитотерапию, электрофорез, лазеротерапию) и постепенное увеличение нагрузки — от простых движений к упражнениям с легкими гантелями или резиновыми лентами.
Боли и дискомфорт в области послеоперационного рубца, сохраняющиеся месяцами, облегчают с помощью специальных гелей и мазей для размягчения рубцовой ткани, физиотерапии (ультразвук, фонофорез) и массажа рубца после полного заживления. Изменения внешности после мастэктомии или реконструкции груди корректируют психологически (работа с телесным образом), подбором специального белья с протезами и, при необходимости, реконструктивной хирургией — одномоментной или отсроченной, с использованием имплантов или собственных тканей (TRAM‑лоскут, DIEP‑лоскут).
Психоэмоциональные нарушения (тревога, депрессия, страх рецидива) требуют консультаций психолога или психотерапевта, когнитивно‑поведенческой терапии для работы с тревожностью, участия в группах поддержки и практик релаксации — арт‑терапии, медитации, дыхательных упражнений. Важен и возврат к социальной активности: постепенное возобновление работы (возможно, с изменением графика или обязанностей), открытое общение с близкими, поиск новых хобби и занятий, участие в благотворительных проектах и группах помощи другим пациенткам.
Побочные эффекты лекарственной терапии также подлежат коррекции: остеопороз на фоне гормонотерапии лечат препаратами кальция, витамина D и бисфосфонатами; хроническую усталость — режимом дня, дозированной физической активностью и полноценным сном; когнитивные нарушения («химио‑туман») — тренировками памяти и внимания, нейропсихологической реабилитацией.
Важную роль играет питание и образ жизни: сбалансированный рацион с достаточным количеством белка (для заживления тканей), клетчатки, витаминов и минералов, ограничение насыщенных жиров и простых сахаров, поддержание нормального веса (избыточная масса тела повышает риск рецидива). Рекомендуются умеренная физическая активность — не менее 150 минут ходьбы в неделю, отказ от курения и алкоголя, полноценный сон (семь-восемь часов в сутки) и профилактика стресса через техники релаксации, хобби, общение.
Обязательная часть реабилитации — диспансерное наблюдение у онколога и маммолога. В первые три-пять лет визиты проходят каждые три-шесть месяцев, включают ежегодную маммографию или УЗИ контралатеральной железы, контроль маркеров (СА 15‑3) при необходимости. После пяти лет ремиссии осмотры сокращают до одного раза в год, ограничиваясь стандартным скринингом по возрасту. При появлении любых новых симптомов (боли в костях, одышка, головные боли, увеличение лимфоузлов) нужно сразу обратиться к врачу.
Грамотно организованная реабилитация помогает не только восстановить функции организма, но и вернуть уверенность в себе, улучшить качество жизни и снизить риск рецидивов. Успех зависит от своевременного начала реабилитационных мероприятий, индивидуального подхода (с учетом объема лечения и осложнений), активного участия самой пациентки и поддержки семьи и специалистов (реабилитолога, психолога, физиотерапевта).
В реабилитации помогают современные технологии: мобильные приложения для отслеживания симптомов и напоминаний о приеме лекарств, фитнес‑браслеты для контроля активности и пульса без перегрузки, телемедицинские консультации для связи с врачом между визитами.
Важно знать «красные флаги» — ситуации, требующие срочного обращения к врачу:
- резкое усиление отека руки или появление отека на другой конечности;
- внезапная одышка или боли в груди (возможны тромбоэмболия, осложнения лучевой терапии);
- нестерпимая боль в костях или перелом при минимальной травме (метастазы, остеопороз);
- лихорадка выше 38 градусов без явной причины (риск инфекции на фоне иммунодефицита);
- изменения на коже рубца (покраснение, язвы, выделения).